我国学者在纳米药物治疗骨关节炎研究中取得进展
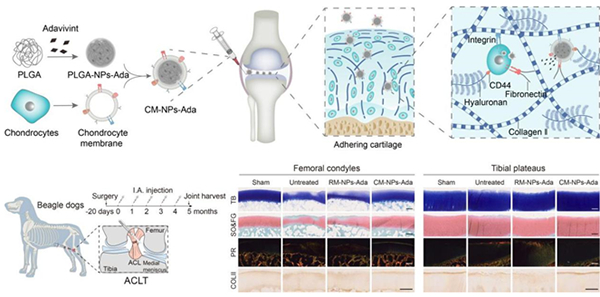
图 仿生软骨细胞纳米药物制备流程、作用机制和大动物疗效评估
在国家自然科学基金项目(批准号:T2288102)等资助下,国家纳米科学中心聂广军团队与清华大学长庚医院余家阔团队合作,在骨关节炎治疗纳米药物库方面取得进展。相关研究成果以“软骨细胞膜修饰的纳米药物在大鼠及犬骨关节炎模型中促进药物滞留并延缓软骨退变(Chondrocyte membrane-coated nanoparticles promote drug retention and halt cartilage damage in rat and canine osteoarthritis)”为题,2024年2月21日发表于《科学•转化医学》(Science Translational Medicine)上。论文链接为:https://www.science.org/doi/10.1126/scitranslmed.adh9751。
骨关节炎(Osteoarthritis, OA)是一种常见的关节退行性衰老疾病,其特征在于关节软骨的进行性磨损、滑膜炎症和病理性软骨下骨重塑,导致患者关节长期慢性疼痛并最终发展为关节功能障碍,目前尚无能够改变OA疾病进程的疗法。尽管一些生长因子、基质金属蛋白酶抑制剂和抗炎小分子在临床前研究中展现出了抑制软骨退化的潜力,但由于难以在软骨组织内维持有效浓度而效果有限。关节内注射药物是提高药物在关节内效果的合理方法,但是面临药物清除快和渗透不足的挑战。因此,需要开发能有效渗透软骨组织并持久留存的药物递送系统,以实现长效治疗。
研究团队受软骨细胞-基质相互作用的特性启发,巧妙利用细胞膜纳米技术,将含有多种软骨细胞外基质黏附受体的软骨细胞膜展示于聚合物纳米颗粒表面(CM-NPs),构建成模仿软骨细胞的纳米药物库。实验结果表明,CM-NPs从纳米尺度模拟了软骨细胞,继承了软骨细胞表面膜蛋白的功能,并主要通过E-钙粘蛋白和网格蛋白介导的内吞及巨胞饮作用,表现出显著的同源靶向性。CM-NPs能够特异性黏附于大鼠及人源退变软骨细胞外基质(ECM),并在大鼠软骨组织内滞留超过34天。体外模拟的滑液清除实验表明,负载Wnt信号通路抑制剂的CM-NPs (CM-NPs-Ada)显著下调了炎症条件下大鼠及人软骨移植物的分解代谢活性。在大鼠及比格犬OA模型中,CM-NPs-Ada有效恢复了模型动物的病理性步态、软骨下骨重塑及有效减缓了软骨组织的退变。总之,该合作团队构建的软骨组织特异性药物储库平台为需要长期药物管理的慢性衰老疾病治疗提供了新思路。


 电话:400-9933-062
电话:400-9933-062 电子邮箱:business@wykt.com
电子邮箱:business@wykt.com

